Bản cập nhật NCCN 2026 đánh dấu một bước tiến quan trọng trong cá thể hóa điều trị: TMB-H (Tumor Mutational Burden – High) chính thức được mở rộng chỉ định trong nhiều loại ung thư rắn, không chỉ giới hạn ở ung thư phổi và melanoma như trước đây.
TMB-H phản ánh số lượng đột biến tích lũy trong tế bào ung thư. Khi số lượng đột biến đủ cao, khối u tạo ra nhiều “tín hiệu lạ” (neoantigens), khiến hệ miễn dịch dễ nhận diện hơn. Vì vậy, TMB-H trở thành yếu tố dự báo đáp ứng mạnh với thuốc PD-1/PD-L1 inhibitors.
NCCN 2026 mở rộng TMB-H cho những bệnh lý nào?
Theo dữ liệu mới:
Ung thư dạ dày
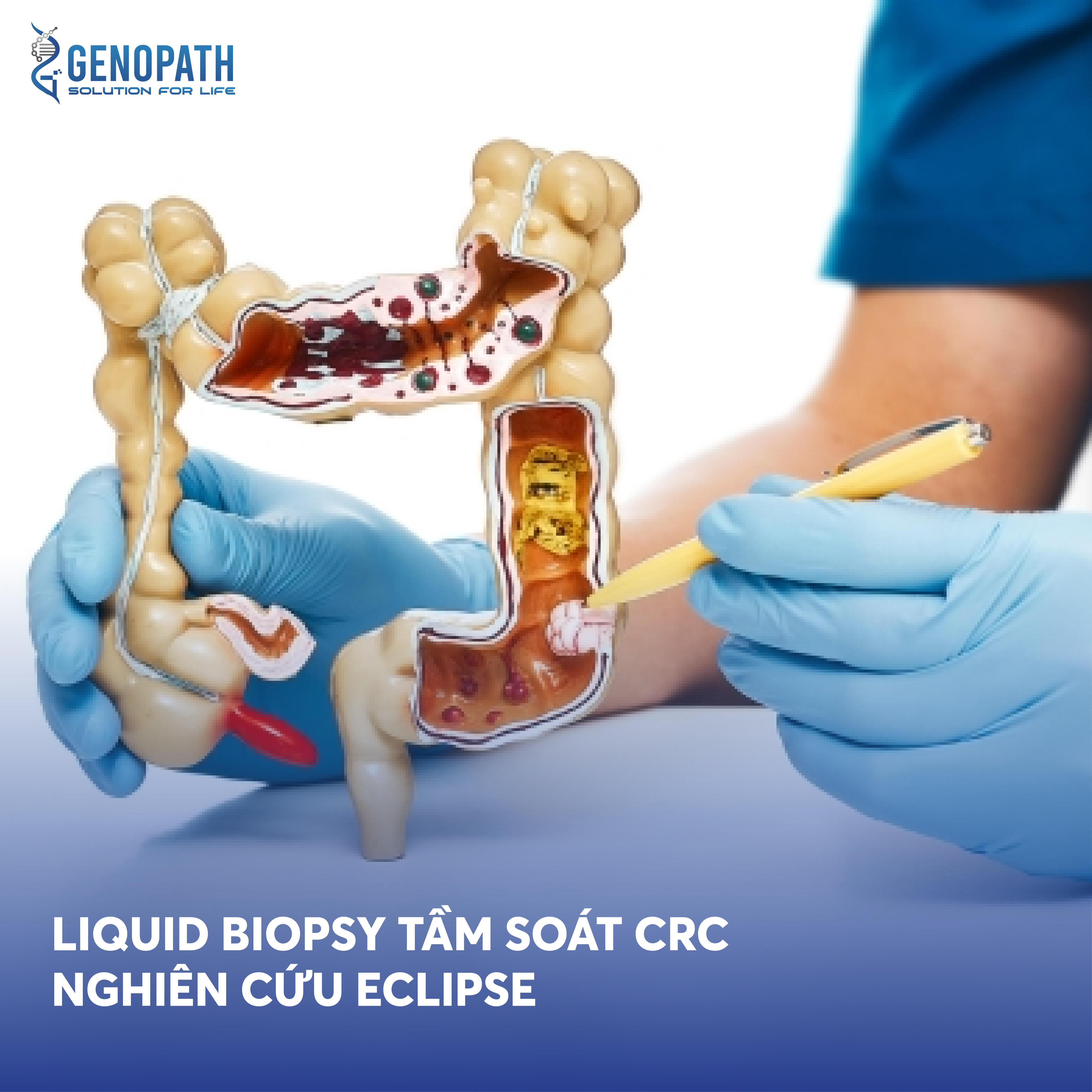
Ung thư đại trực tràng không MSI-H
Ung thư đầu cổ
Ung thư tuyến giáp ít biệt hóa
Ung thư cổ tử cung
Sarcoma và u mô đệm hiếm → Tất cả đều ghi nhận cải thiện tỷ lệ đáp ứng khi TMB-H ≥ 10 mut/Mb (hoặc theo ngưỡng kỹ thuật từng nền tảng NGS).
Vì sao TMB-H tiếp tục được nhấn mạnh năm 2026?
(1) Phân tử hóa điều trị trở thành tiêu chuẩn
Nhiều nghiên cứu tổng hợp 2024–2025 chứng minh rằng TMB-H giúp dự đoán đáp ứng miễn dịch vượt trội ngay cả khi PD-L1 thấp.
(2) TMB giúp chọn bệnh nhân phù hợp hơn
Thay vì chỉ dựa vào mô học hoặc vị trí khối u, TMB cho phép xác định nhóm “immunotherapy-favored”.
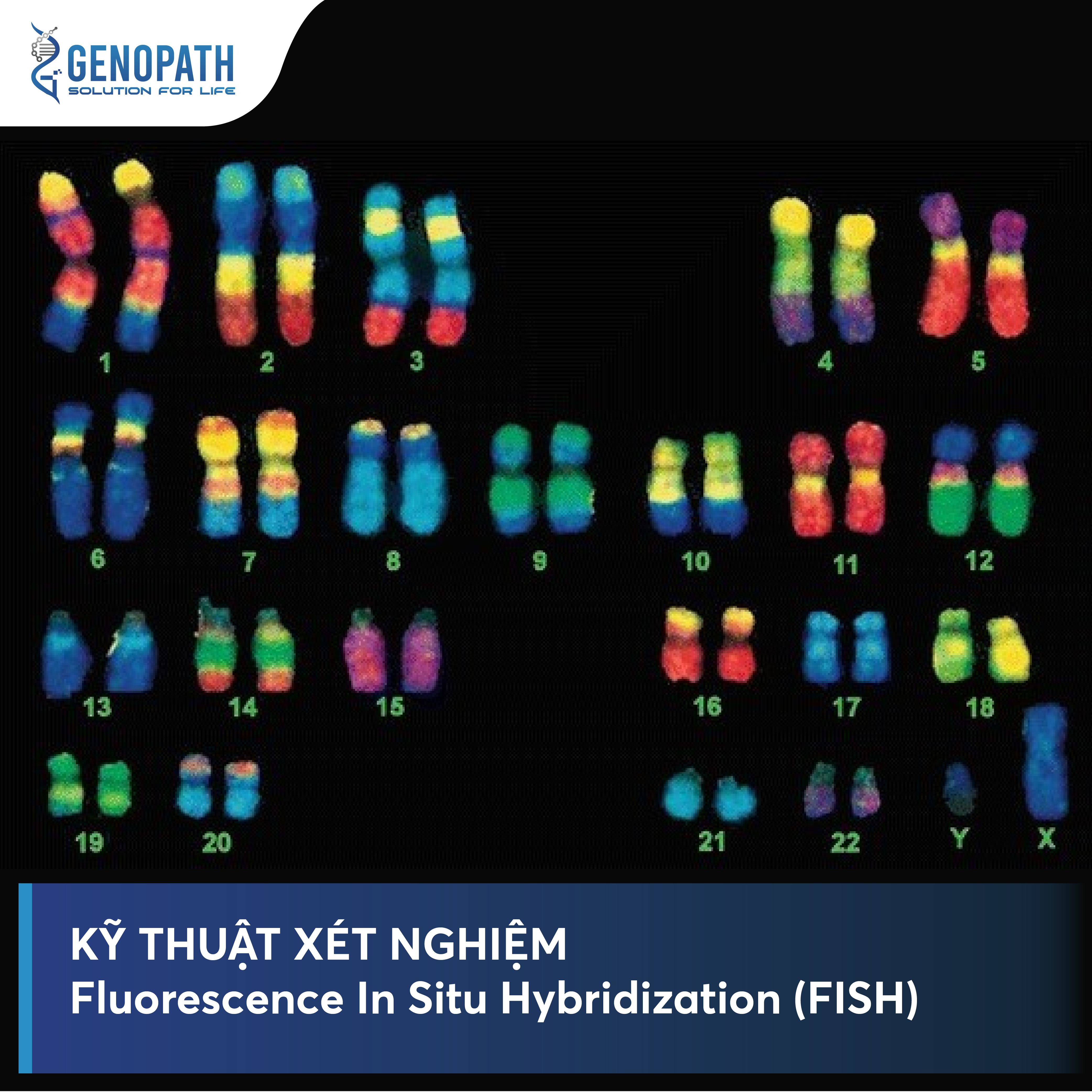
(3) TMB kết hợp tốt với MSI và POLE/POLD1
TMB-H không đứng một mình — nó là phần của bộ ba dự báo miễn dịch:
TMB
MSI-H
POLE/POLD1 ultramutated
Genopath triển khai TMB như thế nào?
Phân tích TMB qua NGS với vùng giải trình tự rộng ≥ 0.8 Mb
Chuẩn hóa kết quả theo nền tảng quốc tế
Báo cáo phân tầng TMB: Low – Intermediate – High
Tích hợp MSI – POLE – PD-L1
Gợi ý tham khảo điều trị dựa trên NCCN 2026
Nguồn ≥2025
NCCN Biomarker Update 2026
ASCO Immunotherapy Framework 2025
Nature Cancer immunogenomics review 2025